■タヒボ、タヒボ茶、健幸堂 タヒボのことなら、私どもにお任せください。■全国送料・代引き手数料無料■

- ホーム >
- ヒト長期摂取臨床安全性試験
ヒト長期摂取臨床安全性試験

タヒボジャパン社では「タヒボNFD」製品の品質と安全性を単に健康食品と位置付けず、医薬品レベルでの管理体制を確立します。その一環としまして、2011年に行われましたタヒボジャパン社の「タヒボNFD」商品群への長期摂取安全性を臨床的な調査と、その結果について紹介します。医薬品を対象にした安全性試験は珍しいことではありませんが、健康食品を対象にした長期にわたる臨床安全性試験は極めてまれで、画期的なことです。本掲載内容は、学術論文誌「日本補完代替医療学会誌 Vol.8 No.2」(2011年)に発表された内容のうち、研究報告者らの許諾を得て、試験結果を中心に抜粋し、再編集して掲載しています。
1.試験概要
【試験目的】
主治療が終了した20歳以上80歳未満の男女60名のがん患者を対象に、タベブイア・アベラネダエ(タヒボ)エキス末の通常量2.0g/日、2倍量4.0g/日、3倍量6.0g/日をそれぞれランダムに6ヶ月間投与し、血液・生化学データ・尿検査・有害事象、各種免疫パラメーター検査、尿中8-OHdG、QOL調査を行った。
タヒボ茶エキス末【「タヒボNFD」エッセンス(タヒボジャパン社)】
※1包(2.0g分包)中、タヒボの樹皮微粉末として5g相当のエキスを含有。
試験実施病院:芳珠記念病院(石川県能美市)
試験実施期間:平成19年9月~平成23年2月
日本補完代替医療学会倫理審査委員会、芳珠記念病院倫理審査委員会において倫理審査を受け承認された。
対象患者は下記の適格基準を満たす者とした。
1)悪性腫瘍であることが組織学的に証明されている患者
2)1)の病名を告知されている患者
3)タヒボ摂取前4週間以内に手術・化学療法・放射線療法・ホルモン療法・BRM(Biological
Response Modifier) 療法を施行されていない患者
4)20歳以上80歳未満の患者
1)摂取量・例数
① タヒボ茶エキス末 2.0g(1包)/日摂取群:20症例(男性10名、女性10名)
② タヒボ茶エキス末 4.0g(2包)/日摂取群:20症例(男性10名、女性10名)
③ タヒボ茶エキス末 6.0g(3包)/日摂取群:20症例(男性10名、女性10名)
2)試験期間
(6ヶ月)+後観察期間(1か月)の計7ヶ月間
3)用法・用量・摂取方法
① タヒボ茶エキス末 2.0g(1包)/日摂取群:
試験開始日から毎日1包(朝または夕)を湯または水に溶かして摂取
② タヒボ茶エキス末 4.0g(2包)/日摂取群:
試験開始日から毎日2包(朝または夕)を湯または水に溶かして摂取
③ タヒボ茶エキス末 6.0g(3包)/日摂取群:
試験開始日から毎日3包(朝・昼・夕)を湯または水に溶かして摂取
・有害事象発現頻度
<血液・尿検査項目>
採血は摂取前、2ケ月目、4ケ月目、6ケ月目、摂取後1ケ月目の合計5回
抹消血液検査:赤血球数、ヘモグロビン、白血球数、血小板数
血液生化学検査:Na、K、Cl、BUN、Cm、AST、ALT、TP、Alb、T-Bil、ALP、γ-GTP、T-cho、CRP
尿検査:pH、蛋白、潜血
有害事象:NCI (Common Terminology Creiteria for Adverse Events version 3.0) 日本語訳 JCOG 版の grade 別副作用発現例数、発現頻度を検討する。
1)免疫検査 (Th1/Th2、NK 活性、Granzyme B、IL-2、IFN-γ、IL-1β、IL-10、IL-12p40、IL-8、
MCP-1、MCP-1、G-CSF)について摂取前、摂取開始2ケ月目、4ケ月目、6ケ月目、摂後1ケ月目
の合計5回測定し比較検討。
測定機関はTh1/Th2、NK活性については(株)エスアールエル、Granzyme B、IL-2、IFN-γ、
IL-10、IL-12p40、ILl-8、MCP-1、G-CSFについては、早稲田大学人間科学学術院鈴木克彦研究室
2)QOL調査は摂取前、摂取開始2ケ月目、4ケ月目、6ケ月目、摂取後1ケ月目の合計5回行った。
3)尿中8-OHdG摂取前の値と摂取2ケ月目の値を比較検討。(株)エスアールエルにて測定。
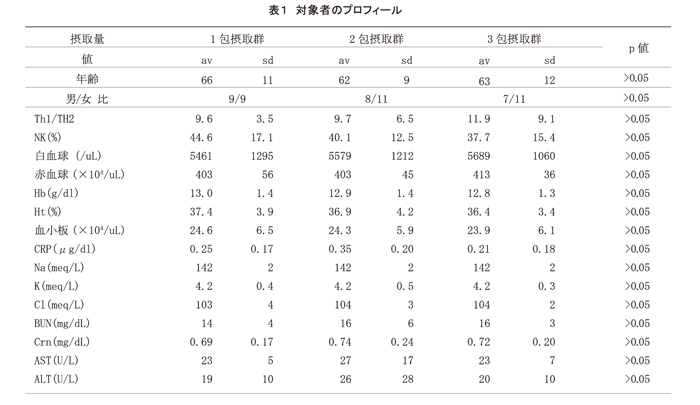
20歳以上80歳未満の男女55名のがん患者で、手術・化学療法・放射線療法などの主治療が終わっている方々。被験者の癌腫は、胃がん19名、大腸がん7名、肺がん5名、乳がん5名、子宮体がん3名、腎臓がん3名、膀胱がん3名、子宮頚部がん2名、卵巣がん2名、食道がん2名、甲状腺がん2名、悪性リンパ腫2名、舌がん1名、前立腺がん1名、白血病1名、皮膚がん1名、膣がん1名。(表1)
2.試験結果
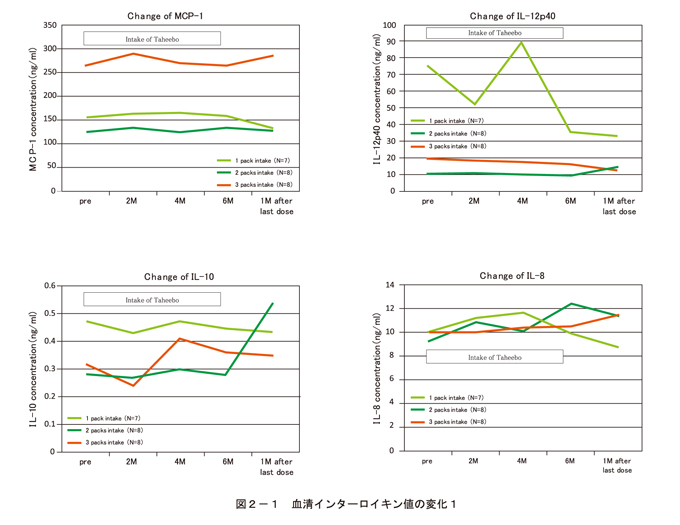
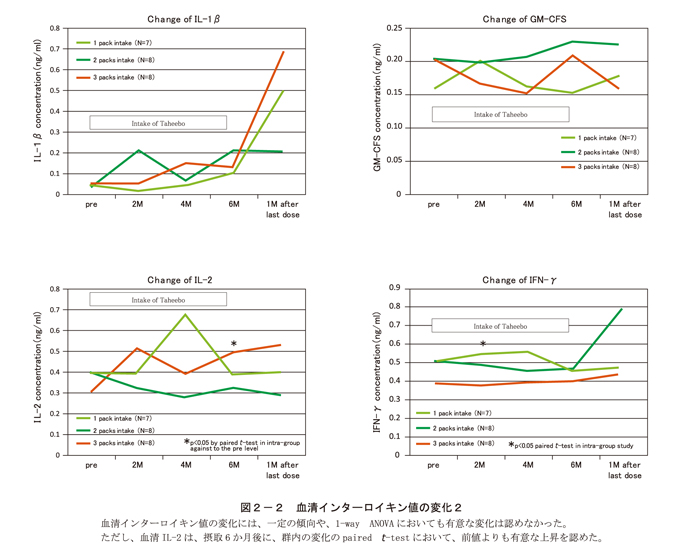
一定の傾向や投与量に依存した変化は認められなかった。しかし、IL-2については、郡内のpaired t-testによって、3包摂取群で6ケ月目に前値と比較して有意な上昇を認めた。(図2-1、図2-2)
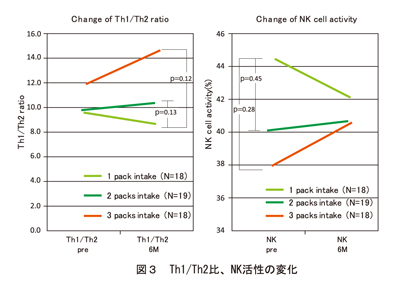
Th1/Th2比、NK活性ともに有意な変化を認めなかったものの、Th1/Th2比の平均値については、摂取量に依存して、Th1/Th2比が上昇する可能性が示唆された。NK活性については、有意な変化は認められなかった。(図3)
Th1/Th2比、NK活性ともに、群間差を2-way ANOVAで検討したが有意な変化を認めなかった。ただし、Th1/Th2比の平均値については、摂取量に依存して上昇する傾向が認められた。
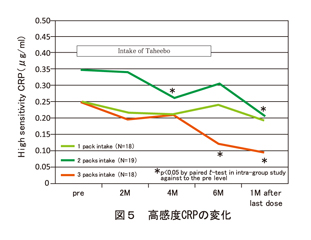
摂取者全員の血清高感度CRPを測定し、平均値を検証したところ、1 way-ANOVAでは有意ではなかったが、paired t-testについては、前値と比較し、摂取量に依存した変化を認めた。特に、2、3包摂取群では、経時的に摂取量に依存した減少を認めた。(図5)
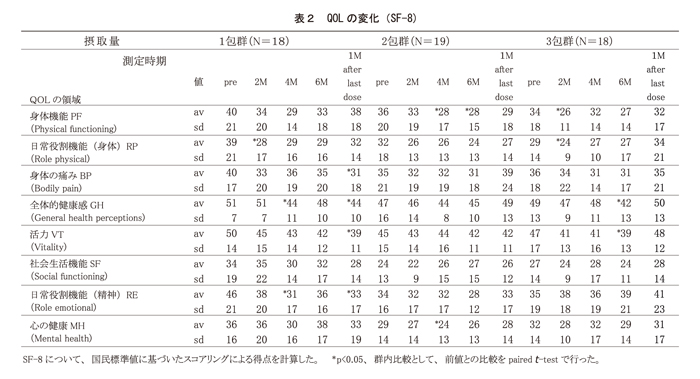
摂取により有害事象(吐き気、めまい、下痢、出血傾向、胃痛、その他生活の質を悪化させる症状)は見られず、また発疹などのアレルギー症状も全く見られなかった。QOLの調査では、日常役割機能の身体面と精神面に関するスコアで、摂取量に依存してQOLが向上している可能性が示唆された。特に精神面の日常役割機能は、1包摂取で2ケ月目に悪化するものの、2、3包摂取群ではその悪化が認められなかった。(表2)
3.考察
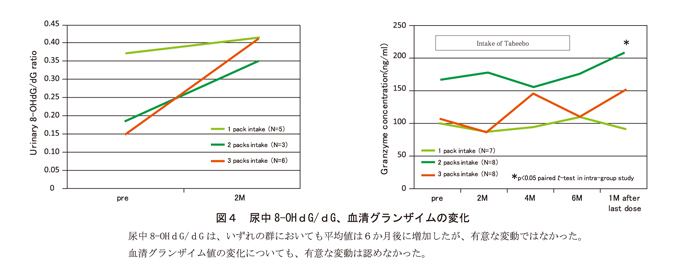
血清アルブミン値は、タヒボ茶エキス末摂取量に依存して低下が抑制されており、摂取を終了すると1ケ月後には有意に低下していることから、タヒボ茶エキス末が、がん患者の栄養状態の低下を抑制していた可能性が推定された。しかし、同じ栄養状態の指標とも考えられるHb値については、3包摂取で正常範囲内での低下傾向を認めた。Hbの低下については、栄養吸収の低下によるよりも、造血系への直接的な作用によるものかもしれないが、はっきりとした原因は不明である。
血清サイトカイン値やNK活性など免疫機能には、一定の傾向は認められなかった。タヒボの免疫系の作用は基礎実験では実証されていることから、今回の結果は、いろいろな病態のヒト試験における問題点として、さまざまな要因による個体差などが出現したためと思われる。
腎機能異常で摂取を中止し脱落した被験者(77歳女性:表1)は、原病として糖尿病性腎症を有し、タベブイア・アベラネダエ摂取以前にも、時々クレアチニンが上昇した既往を持つ例である。本例は、adverse eventに分類したが、タベブイア・アベラネダエ摂取が原因とは断定できない例であり、因果関係は不明と判定した。また、上記症例と同じく、慢性腎臓病(CDK:Chronic Kidney Disease)の被験者(59歳女性:表1)は、本食品摂取以前から尿潜血が3ケ月以上時々+もしくは±となっていた患者であるが、今回摂取中に3+となり、摂取を中止し脱落例となった例である。本例もadverse eventに分類したが、本食品摂取が直接の原因とは断定できない例であり、因果関係は不明と判断した。
なお、今回の55例での解析において、腎機能の指標であるBUNやクレアチニン値については、摂取量に依存した一定の傾向は認めなかったので、本食品と腎障害との因果関係はないとみなしたが、上記2者は、腎機能に注意して摂取することが肝要と思われた。血清高感度CRPは、タヒボ茶エキス末摂取量に依存して低下を認めた。確かさは弱いが、動脈硬化性病変や血管内皮細胞機能、全身的な炎症状態について、タヒボが改善する作用を有することが推定され、今後の研究に期待が寄せられる。
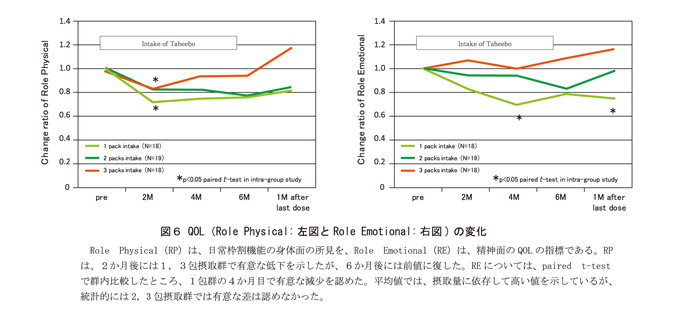
QOLについては日常役割機能の身体面(RP)と精神面(RE)に関して、1、2包ではQOLが悪化した一方で、3包群では悪化が抑制されたQOLの領域があった。アルブミンや高感度CRPなどの変化と合わせて考えると、容量依存的にがん患者の低下するQOLを上げる働きを表している可能性もある。(図6)
4.結論
タベブイア・アベラネダエ(タヒボ)の通常量、2倍量、3倍量摂取は有害事象を起こすことなく、血液生化学的な改善作用やQOLの低下の抑制作用なども認められ、臨床上安全な食品であると考えられる。また、タヒボ食品3包での、がん患者での栄養低下の抑制、高感度CRPの低下作用などのこれで報告されなかった効果が本研究により示唆された。
 072-235-3364
072-235-3364 072-235-3365
072-235-3365